不同生产工艺的玻尿酸差别
文章来源:AVT发布时间:2022-07-27浏览次数:
不同生产工艺的玻尿酸差别
一、 玻尿酸总述
玻尿酸(HA)是一种由N-乙酰氨基葡糖和D-葡糖醛酸的重复结构组成的线性多糖结构分子,这种结构来源于HA的生物合成途径,HA在生物体内合成过程中,经过多种糖基转移酶和有关修饰酶的作用,形成有特定顺序的重复单位的线形分子。从其结构上可以看出,由于直链轴上的基团之间的氢键作用,HA分子空间结构为二折体或三折体的螺旋结构,玻尿酸的二折体或三折体螺旋结构进一步折绕,形成特有的三级结构,赋予其弹性。同时葡萄糖醛酸残基上的羧基使它一具有特殊的粘性,较多的亲水基团和疏水区域使其有优异的保湿功能。因此玻尿酸作为构成人体细胞间质、眼玻璃体、关节滑液等结缔组织的主要成分,在体内发挥保水、维持细胞外空间、调节渗透压、润滑、促进细胞修复的重要生理功能;同时玻尿酸能使皮肤、血管等保持柔韧性和弹性,是生命体不可缺少的物质之一。
目前关于玻尿酸的生产工艺,在工业生产上主要有组织提取法和微生物发酵法两种工艺,下面我们就这两种工艺基本情况的介绍以及不同玻尿酸获取工艺的特点,做一个详细的介绍。
二、 动物组织提取工艺生产玻尿酸
2.1 工艺原理
玻尿酸是构成细胞外基质(ECM)和细胞间质(ICM)的主要成分,在动物的各种组织中广泛存在,如动物的结缔组织、脐带、皮肤、血清、鸡冠、关节滑液、眼玻璃体等部分都存在不同含量和不同平均分子量的玻尿酸,其中在脐带,关节液、玻璃体和鸡冠中的透明质酸含量是最高的。
玻尿酸的组织提取法工艺就是利用高HA含量的动物组织作为提取原料,在蛋白酶(胰酶、木瓜蛋白酶及碱性蛋白酶)的酶解作用下,使HA与蛋白质分离从而将HA提取出来,随后经过除杂、沉淀和分离等工艺后,即可得到HA粗产品,再经过反复纯化处理即可得到精制HA原料。
2.2 工艺过程
透明质酸的组织提取法主要是从鸡冠、动物脐带、动物眼球等组织中提取,在工业化生产中,一般采用酶解法进行HA的制备。我们以鸡冠为原料,采用酶解组
织提取法工艺为例,详细介绍动物组织提取工艺生产玻尿酸的工艺过程。
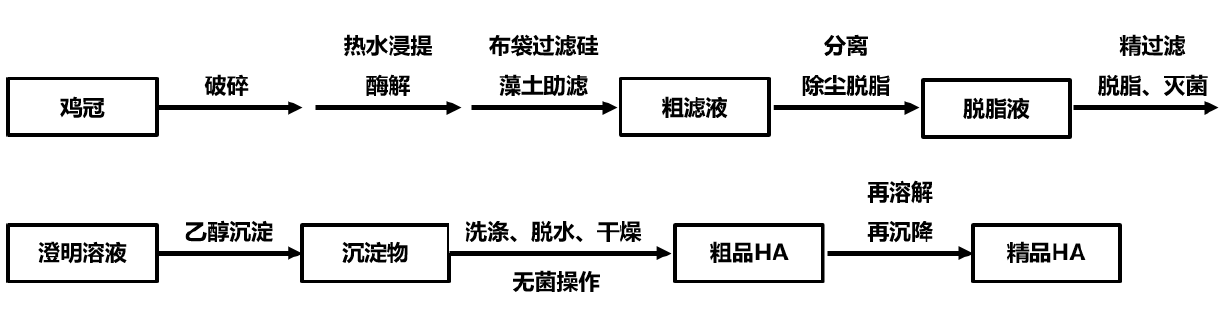
图1:鸡冠提取玻尿酸生产工艺路线
2.2.1 鸡冠原料处理
鸡冠富含HA,工业上使用鸡冠原料提取HA时,玻尿酸的收率一般可达数g/kg。在使用鸡冠提取玻尿酸时,首先需要通过冻融、丙酮浸泡等方式对动物组织进行预处理,分离得到HA含量较高的动物组织。然后用绞肉机或合适工具绞碎物料,最后经研磨等匀浆化,制成匀浆。为便于匀浆化,解冻脱血水后可用80~ 90 ℃水处理0.5~ 1 h,使物料呈“半熟”状态,这使蛋自质变性,组织所含酶失活,对后续蛋白质酶解有利。
2.2.2 酶解蛋白提取或无机盐/碱萃取HA
通过胰酶和碱性蛋白酶对匀浆进行酶解,蛋白质被酶解,蛋白质与HA的络合被解除,从而使HA与蛋白分离开,此时HA即可溶入水中。酶解并不是要求将蛋白质降解为氨基酸,而是尽可能完全地使络合物离解出HA来。可使用各种蛋白水解酶,如胃酶、胰酶及许多微生物酶,根据酶活性和特性的不同,加入5~ 50万U/kg组织的酶量,将温度和pH值调到酶具有最高活性的值,保温数小时至一天,酶可一次加入,也可分批加入。
无机盐或无机碱可以使HA与蛋白质等的络合状态解除,因此采用无机盐或无机碱也可以从鸡冠中萃取出HA,工业上常用0.1~ 0.5M的氯化钠溶液对匀浆进行处理,也可用0.1M的氢氧化钠溶液萃取鸡冠、脐带中的HA,需要注意的是,过分剧烈的化学条件可能会造成玻尿酸的降解和变性(乙酰氨基水解),因此在使用无机盐或无机碱时,需要控制好提取条件。
2.2.3 过滤分离除杂
萃取或酶解所得混合物经压滤或离心分出HA溶液,抽滤会形成大量泡沫,操作有困难。制高纯产品时,滤液须再用氯仿脱色,用丙酮脱脂,用蛋白酶分解残存蛋白质,或者通过三氯乙酸沉淀等方法去除杂蛋白。
2.2.4 沉降HA
过滤得到的玻尿酸溶液浓度很低,用浓缩法不能回收HA,只能用沉降法。目前有乙醇法和十六烷基盐酸吡啶法两种。其中,乙醇法中常用1~3倍体积乙醇沉淀,HA在由此形成的醇水介质中难溶,沉降很彻底。N -十六烷基盐酸吡啶水溶液的浓度为5%,用量视滤液浓度而定,可为滤液的5%~ 10%(以100%计)。它能与透明质酸反应,形成不溶于水的透明质酸-N -十六烷基吡啶盐而沉淀。
2.2.5 精制HA
沉降的HA含有蛋白质、其它粘多糖等杂质,常需净化精制。精制包括再溶解、再沉降。精制可以提高纯度,但会造成HA原料的损失、降低收率。如需更高纯度,要重复进行再溶解和再沉降。最多可反复5次,这时产品纯度很高,但收率下降,甚至不足1 g/kg组织。
再溶解使用两种溶剂,0.1N的氯化钠溶液或30%~ 40%乙醇溶液为溶剂的0.5 N的氯化钠溶液。滤除不溶物后用95%乙醇进行再沉降。然后用乙醇洗涤,以除去吸附水,最后采用真空干燥对HA原料进行烘干。
纯度较高的HA要求蛋白质含量小于0.1%,高纯产品,特别是植入类玻尿酸产品,质量标准十分苛刻,必须达到较低的杂蛋白,无热源,较高分子量等,按此要求,最终得到透明质酸量约为鸡冠重量的0.1%,自然注射级HA的价格也就更高。
2.3 工艺特点
透明质酸的组织提取法过程包括脱水、磨碎、浸泡、提取、除杂、沉淀和分离。这种方法的特点是工艺流程简单,获得的透明质酸分子量较大,粘度高,保湿性能好,适用于原料来源分散的小规模生产。但由于原料有限,且原料中HA 的含量低,同时HA 又还与硫酸软骨素等粘多糖共存于生物组织中,致使其收率低、提纯难、成本过高、产品质量差,且难以应用于大规模生产。另外用生物原料提取的HA常含较多的蛋白质而纯度不高。在提取过程中使用三氯乙酸变性沉淀蛋白质还会造成分子量的下降。用这种方法HA时,分子量、产率和纯度之间存在矛盾。除此之外,动物源制品容易成为病毒传播的载体,会有引起交叉感染的风险。
三、 微生物发酵工艺生产玻尿酸
3.1 发酵工艺原理
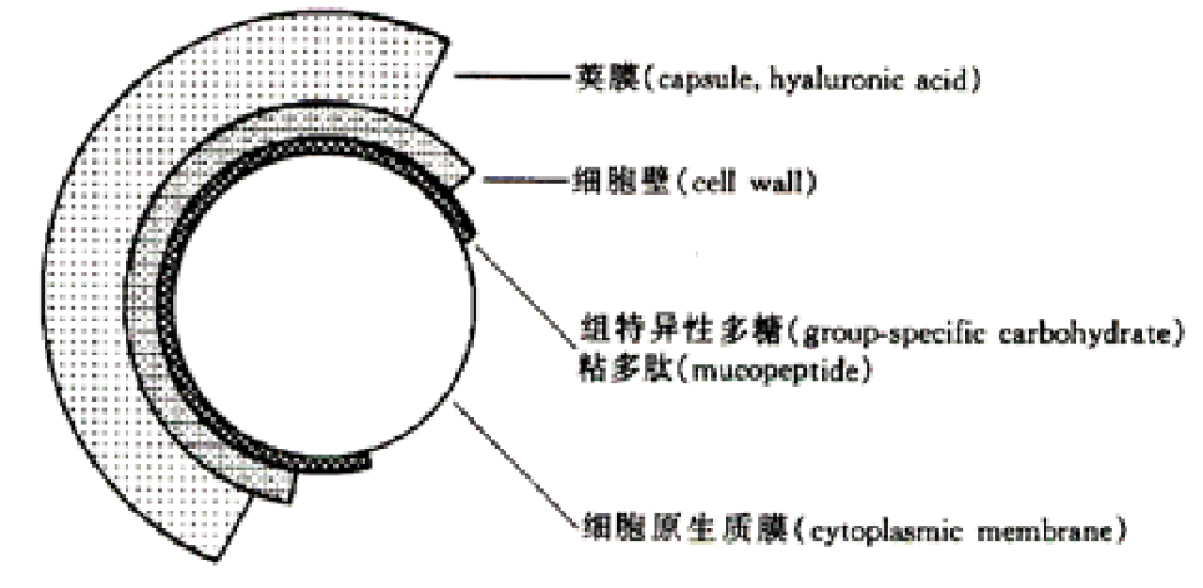
图2:链球菌荚膜示意图
微生物发酵法主要用的菌种为链球菌,玻尿酸的合成主要在链球菌体的细胞基质和细胞膜上进行,是一个连续而又复杂的过程,HA的两个合成前体是尿苷二磷酸-N-酰基-氨基葡萄糖(UDP-N-Glc NAc)和尿苷二磷酸-葡萄糖醛酸(UDP-Glc A)。在玻尿酸的合成过程中,HA合成酶交替地将两种前体物质添加到HA分子链上,合成速度每分钟大约100个糖单位。与此同时,逐渐增长的HA链会被送到胞外基质中,因此链球菌属的多种细菌的荚膜都有大量的HA成分,如图2所示。而微生物发酵法则就是利用链球菌在生长繁殖过程中,向胞外分泌以HA为主要成分的荚膜,而后通过分离纯化而制备得到HA。
3.2 发酵工艺过程
由于HA 具有特殊的功能及广泛的用途,规模化生产HA 十分必要。如果仅依赖于从动物组织中提取,很难满足市场的需求。而发酵法生产HA 成本低、产品纯度高、易形成规模化生产,具有广泛的市场应用前景,采用链球菌发酵生产HA的工艺流程如下:
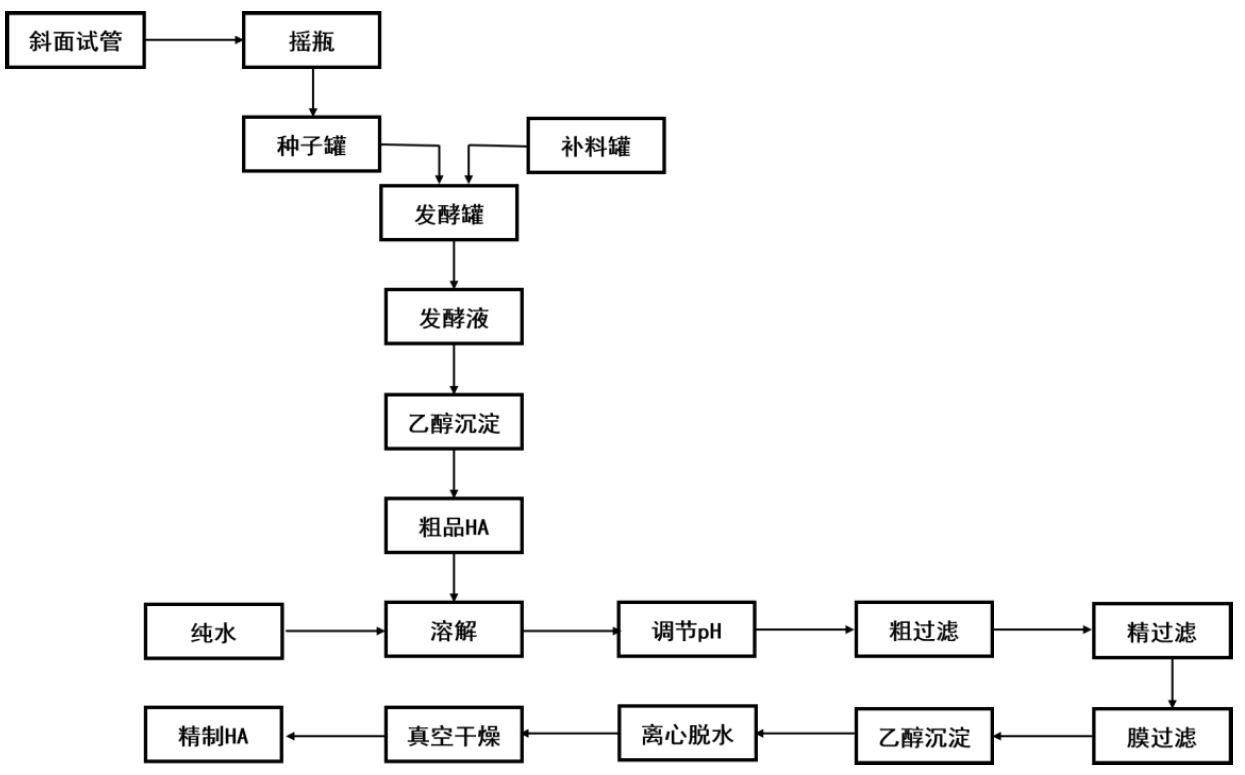
图3:链球菌发酵生产HA工艺流程
兽疫链球菌在适当的条件下发酵一段时间,所用的碳源主要有葡萄糖、蔗糖、果糖、淀粉等,氮源主要有蛋白胨、酵母浸出粉、牛肉膏等,以及常用的无机盐,如K2HPO4、MgSO4、NaCl等。发酵完成后,将发酵液离心去除兽疫链球菌的菌体。上清液加入乙醇醇沉后得HA粗提物。之后可以用离子交换剂或者加入氯化十六烷吡啶(CPC),再经过在氯化钠溶液中的析出与溶解,除去兽疫链球菌代谢生成的蛋白质、游离的核酸和其他的菌体杂质性产物等。最后经过醇沉、离心和干燥后,可以得到精制HA。
利用微生物发酵生成HA 的质量和数量主要取决于三个方面:一是菌种的筛选,二是培养基的选配及发酵工艺的优化,三是分离提纯。发酵法的关键在于菌种的选择,可产生HA 的链球菌多为A群和C群,A群中主要有酿脓链球菌等,由于致病性较强,较少用作菌种进行大规模发酵;C群致病性较弱,多采用此类菌,主要有兽疫链球菌、马链球菌和类马链球菌等。发酵生产HA 所用的菌种,一般是将产生HA 的链球菌进行诱变处理得到的,经过几步诱变处理,筛选出荚膜大、HA 产率高、无HA 酶和溶血素的变异菌株。
目前国内HA的发酵产率为4~5g/L,从发酵液到最终产品的纯化收率为60%~70%。发酵工艺优化是提高目标产量所必需的的一个步骤。通过优化菌株的培养基以及培养条件,可以使透明质酸的产量得到稳定提高。筛选的菌株在以蔗糖或者葡萄
糖为碳源,酵母粉、牛肉浸膏等为氮源的培养基中培养,控制培养过程中的温度、溶氧条件、搅拌速度等因素,而且在发酵过程中会产生乳酸,这将会抑制透明质酸的生成,同时也会抑制菌体的生长。因此在发酵过程中,还要抑制乳酸的生成,如此结合才可以得到富含透明质酸的发酵液。
3.3 发酵工艺特点
微生物发酵法生产规模不受动物原料限制,无动物来源的致病菌污染,具有低成本、髙产量和高分子量的优点,并且发酵液中HA以游离状态存在,易于分离纯化和形成规模化工业生产,逐渐成为透明质酸生产的主要发展方向。而且各种来源的HA 无种属差异,不同动物组织提取及不同菌种发酵生产的HA,在化学本质和分子结构上是一致的,只是相对分子质量有差别。
然而由于发酵液中含有大量的菌体,这些菌体可以分泌一种可解离HA的透明质酸酶,降低HA分子量,从而影响到HA产品的质量,所用进行下游分离纯化时,必须尽快杀灭和除去发酵液中的菌体,并使酶失活。同时发酵液中的HA含量高、分子量大,所以发酵液的粘度很高,这就给分离的过程带来许多不便,如不能用离心法除菌体,收率会因HA的黏附而降低等。最后,由于对HA产品分子量有十分严格的要求,而HA易因酸、碱或加热处理而分解;在铁、铜等金属离子和抗坏血酸或半胱氨酸等还原剂共存下,经氧自由基、X射线、Y射线、紫外线和超声波作用而降解;它还可被透明质酸酶和硫酸软骨素酶分解。因此,对HA的提取就要求在分离纯化的同时,严格控制条件,减少HA分子的降解,保证产物的高分子量。
四、动物组织提取法和链球菌发酵法生产HA的对比
|
项目 |
组织提取法 |
链球菌发酵法 |
|
原料来源 |
特定部位的动物组织,难以大量收集 |
常用的碳源和氮源培养基,容易得到 |
|
存在状态 |
与蛋白质、糖胺聚糖等形成聚合体 |
游离于发酵液中 |
|
产率 |
与原料部位和提取率相关,不稳定 |
与发酵规模有关,稳定无限 |
|
成本 |
高 |
低 |
|
分离纯化 |
操作复杂,使用大量有机溶剂和蛋白酶 |
操作简单,使用助剂少 |
|
相对分子量 |
取决于动物组织部位,不可控,一般在(0.1~ 2.5)×106 |
可通过培养条件进行调控,一般在(1.0~ 4.0)×106 |
|
品质纯度 |
受原材料影响,易含杂蛋白 |
含杂质更少,纯度更高 |
|
安全性 |
存在动物源性风险 |
无动物源性风险 |


