《mRNA-LNP疫苗的结构与稳定性》文献解读系列三
文章来源:AVT发布时间:2021-08-31浏览次数:
LNPs 作为递送系统
为了克服裸露的mRNA转染的种种问题,已经开发了保护性递送系统。目前的mRNA疫苗(表 1)都在使用 LNP 技术。这说明了使用LNP能在稳定mRNA 的同时并将其递送到细胞中。mRNA疫苗中的LNP 由四种主要成分组成(见表1):中性磷脂、胆固醇、聚乙二醇 (PEG) 脂质和可电离脂质。可电离脂质含有带正电荷的可电离胺基团(在低 pH 条件下电离),可在颗粒形成过程中与阴离子mRNA 相互作用,并在细胞摄取过程中促进膜融合。此外,PEG化脂质用于控制粒径并充当空间屏障起稳定作用,防止储存过程LNP微粒聚集。通过使用微流控混合生产技术,这些脂质成分与 mRNA 一起形成大小约为 60-100 nm 的颗粒。例如,SARS-CoV-2 候选疫苗nCoVsaRNA和ARCoV的平均粒径分别为75 nm和89 nm。
表一:
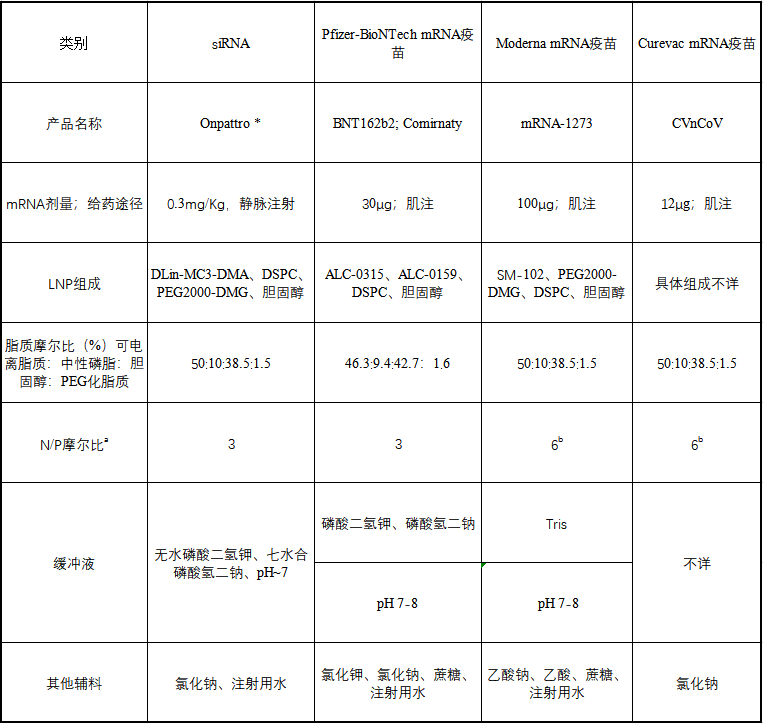
LNPs与脂质体的不同之处在于微粒中存在脂质,来自几项研究的数据表明水也存在于微粒内部某些空间。这意味着mRNA即使被包封也可能暴露于水性环境中。这种类型的内部结构,先前已在未包载和包载siRNA的LNP中被冷冻电镜所观察到。类似地,mRNA-LNPs 的冷冻电镜结果也显示了电子致密核,劳氏紫(Thionine)对RNA进行染色用于冷冻电镜对比度增强(见图2)。
尽管mRNA-LNP 的共同特征是脂质,但该的确切结构特征及其对脂质成分(摩尔比)和 mRNA 定位的依赖性仍存在争议(见图3)。正如 RiboGreen检测实验所确定的那样,mRNA 肯定位于 LNP 内部。RiboGreen 是一种染料,当与单链 mRNA 结合时会显示荧光,但不能进入 LNP。在 mRNA-LNP 制剂中,例如mRNA 疫苗的制剂,可与RiboGreen结合产生荧光的mRNA 比例非常低,因此,采用RiboGreen来测定的包封率通常 > 90%。综上所述,冷冻电镜(图2) 和包封率证据表明,mRNA-LNPs形成纳米粒子,其中包封了 mRNA,可免受外部介质的影响,LNPs包封的mRNA的结构有3种模型,这些主要来源于siRNA-LNPs分析(图3)。

图2 mRNA-LNP 的冷冻电镜图像显示具有明显不同电子密度的“囊泡”结构
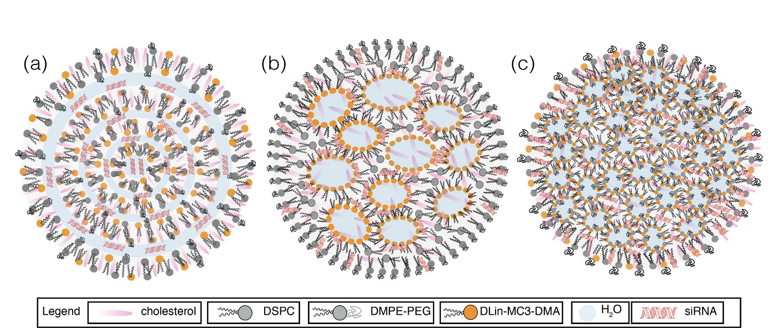
图3 siRNA-LNP 和 mRNA-LNP 结构的推测模型的示意图 A:多层囊泡;B:纳米结构核;C:均质核壳
mRNA疫苗所包封的mRNA会影响终LNP的结构:siRNA 在结构和分子量大小上与 mRNA 有很大不同(表 2)并且N/P(可电离的阳离子脂质与核苷酸磷酸盐)摩尔比不同,N/P摩尔比分别为3和6(表 1)。mRNA 至少比 siRNA 大 100 倍,这会影响 LNP 的结构。此外,有迹象表明 mRNA 位于 LNP 的核,而siRNA 更靠近表面,mRNA 可以形成“囊泡”(图 2)。LNP 囊泡部分的组成是一个有争议的问题,在这种状态时:“mRNA 可以从带电的脂质中解离,留在充满溶剂的囊泡隔室中”。
表2 mRNA 和siRNA分子之间的差异
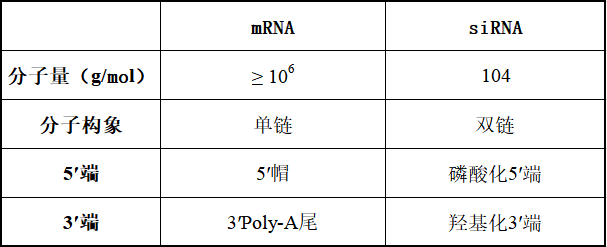
mRNA-LNP不太可能是(图 3A)的多层囊泡模型。它与mRNA-LNP的 TEM结果中电子致密核位置不对应。目前,大多数研究人员认为 mRNA-LNP 贴近核壳模型(图3 B和C),这意味着纳米颗粒具有表面层和无定形的各向同性核。Viger-Gravel等,使用核磁共振光谱证明LNP结构的两种类型的核是可能的。
他们描述了一个被阳离子脂质包围(图3B)的包含水孔的无定形核模型。他们还假设核中的脂质可以均匀分散,中间有“小水球”(图 3C)。后者(图3B和C)跟siRNA-LNPs和mRNA-LNPs在实验观察到的结果更吻合。
Arteta等人,使用冷冻电镜、小角 X 射线散射 (SAXS) 和小角度中子散射 (SANS) 测量 mRNA-LNP 结构模型。他们发现DSPC和PEG化脂质以及部分可电离的阳离子脂质和胆固醇是位于LNP 的表面,可电离的阳离子脂质、胆固醇(取决于其浓度)、水和 mRNA 的主要部分分布在核内部。有趣的是,他们的研究表明,各向同性LNP 核由24%(体积分数)的水组成。他们指出 mRNA 位于水柱内,水柱被阳离子脂质包围(如图4所示)。这意味着 mRNA 至少部分暴露于LNP 内部的水中,这可能导致mRNA在非冷冻条件下储存时不稳定,Sebastiani等人也报道了类似的结果。
因此,研究 mRNA 如何与 LNP 中的水和可电离的阳离子脂质相互作用是一件很有趣的事。mRNA 是亲水的,它可以通过静电和氢键与可电离的阳离子脂质相互作用(通常表观pKa < 6.5)。这取决于 LNP 内部的pH值,如果 LNP 外壳对质子具有渗透性——这很可能,因为 2-(对甲苯胺基)-6-萘磺酸 (TNS) 和劳氏紫等离子化染料可以进入 LNP 核,那么LNP内部的pH值与制剂的其余部分应该相似,约为7 到 8,这意味着大多数可电离的阳离子脂质将不带电。
然而,由于可电离的阳离子脂质堆积在核中,它们可能表现出聚电解质行为,导致 Henderson-Hasselbalch 方程的偏差,即滴定曲线的“拖尾”(脂质膜内的可电离脂质的表观pKa可能与实际值有较大偏差,这意味着pKa为6.5左右的可电离脂质在脂质膜内的表观pKa可能与理论值有1~2个pKa单位的偏差,所以pKa为6.5左右的可电离脂质在pH值为7-8之间的脂膜内时,依然有可能绝大部分呈现带正电的状态,注:红色斜体部分是对一些较复杂概念的进一步解读,后同)。此外,mRNA 和可电离的阳离子脂质之间的相互作用可能会影响电离行为。
对于 siRNA,发现与可电离阳离子脂质存在较弱的静电相互作用,这表明至少对于 siRNA-LNP 制剂,内部的pH值接近或等于外部的pH值。对于 mRNA-LNP,尚未进行此类实验研究。mRNA 和阳离子脂质复合的分子动力学模拟研究证明了脂质-脂质簇和脂质-mRNA 簇的形成。静电力和氢键都在驱动阳离子脂质和 mRNA 的相互作用。
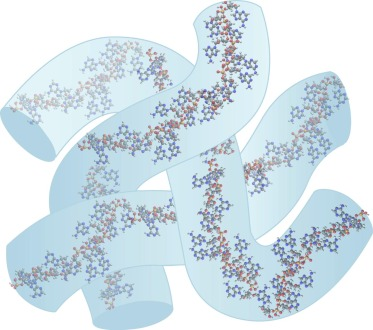
图4 mRNA-LNPs核中mRNA-水柱的示意图
Arteta 等人的另一个有趣发现是他们的mRNA-LNP 的外壳是单层的。其他研究人员根据冷冻电镜(图 2)或 SANS结果分析提出,mRNA-LNPs 的外壳由一个或多个双层组成。这些相互矛盾的发现表明,使用这些技术评估mRNA-LNP 壳的性质是困难的,可能存在多种类型的mRNA-LNP 结构,其结构取决于脂质的性质和mRNA-LNP 的制备方法。反过来,不同的结构可能会对不同配方的稳定性产生影响。总之,问题仍然在于目前我们尚不清楚 mRNA-LNP 的结构以及包封的mRNA 与各种脂质成分之间的相互作用。
对各种 mRNA疫苗成分的分析表明,它们具有共同特征,但也存在差异(表 1)。LNP 配方、修饰核苷的使用、高GC含量以及常规 mRNA 和 SAM 疫苗之间的长度差异可能会影响这些 mRNA疫苗在储存过程中的物理和化学稳定性。
1、中文名称:DLin-MC3-DMA
2、商品名:DLin-MC3-DMA
3、化学名称:4-(N,N-二甲基氨基)丁酸(二亚油基)甲酯
(6Z,9Z,28Z,31Z)-heptatriacont-6,9,28,31-tetraene-19-yl 4-(dimethylamino)butanoate
4、分子式:C43H79NO2
5、生产商/manufacturer艾伟拓(上海)医药科技有限公司/ AVT (Shanghai) Pharmaceutical Tech Co,. Ltd.
6、CAS号:1224606-06-7
7、用途:阳离子脂质体
8、结构式: 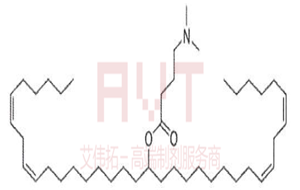
9、性状:无色至淡黄色油状液体
10、纯度:98%
11、溶解性:不溶于水,易溶于DMSO、甲醇、乙醇。
12、分子量:642.09
13、保存条件:-20℃
14、注意事项:避免与强酸、强碱、强氧化性物质接触
15、货号:002006


