记录蔗糖八硫酸酯在冷冻电镜中的一次出镜
文章来源:AVT发布时间:2021-12-09浏览次数:
2021年4月15日,《cell》第8期184卷上刊出文章“Simultaneous binding of Guidance Cues NET1 and RGM blocks extracellular NEO1 signaling[1]”
摘要: 在细胞迁移和分化过程中,细胞的表面受体可以同时结合不同的配体,然而,对于如何整合这些细胞外信号的了解却比较少。当Netrin-1(NET1)结合配体时,Neogenin(NEO1)会充当具有吸引力的引导受体,但它也会通过排斥性导向分子(RGM)介导排斥。文章揭示,通过三元聚合物(NEO1-NET1-RGM)复合物的形成进而整合了细胞外的信号并触发了下游信号的相互沉默。作者通过NEO1-NET1-RGM结构揭示了存在于细胞膜中的“三聚体”超级组装,并且这个超级组装形成的三聚体会通过阻断RGM-NEO1复合物形成的信号以及NET1诱导下的NEO1胞外聚集,进而抑制RGMA介导的生长锥塌陷以及RGMa或NET1-NEO1介导的神经元迁移。这些结果验证了当两个具有相反功能的配体与单个受体同时结合时,不会导致竞争性结合,而是会形成降低其功能的超级复合物。
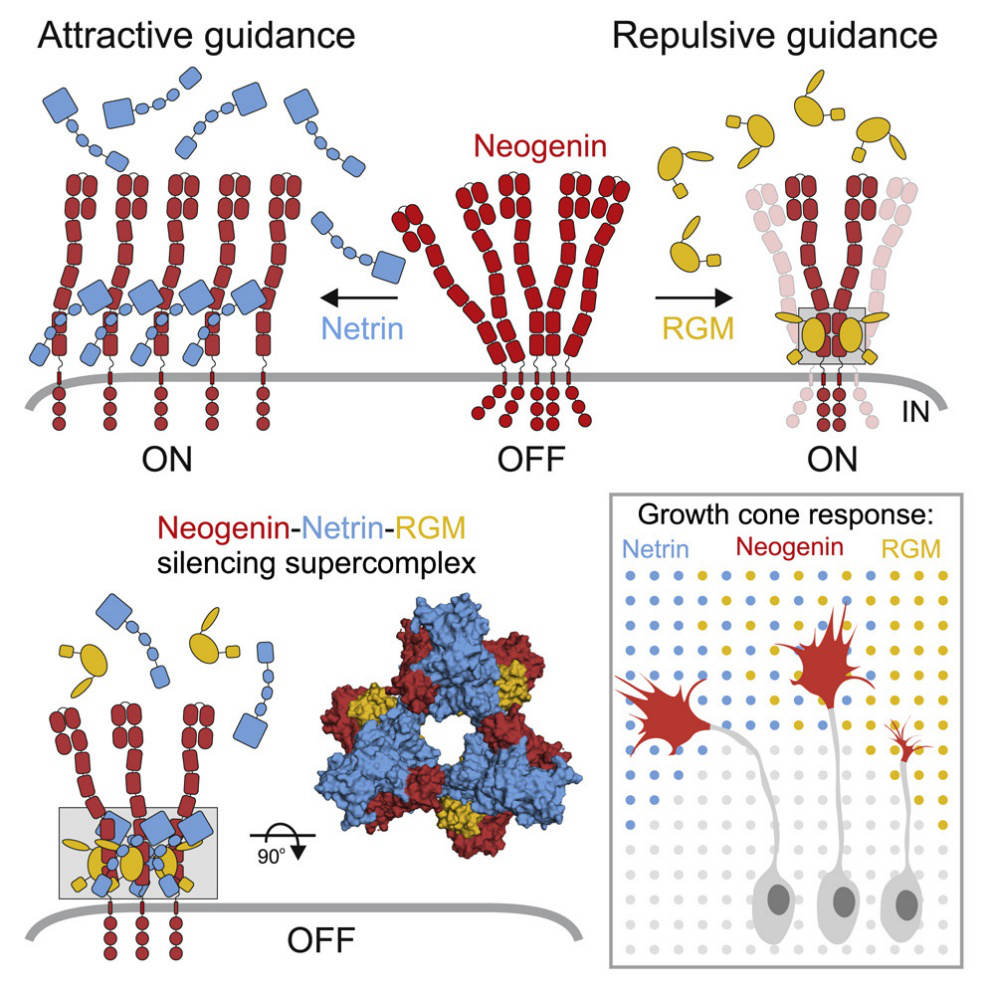
图1. “3-3”聚合体的作用示意图
结果:为了剖析通过RGM和NET1相互作用控制NEO1信号传导的分子机制,作者使用了表面等离子体共振(SPR)以及细胞表面结合实验确定了NET1-NEO1相互作用的最小结合区域,测试表明,最小复合物由NEO1的三个靠近膜的FN结构域(NEO1FN456)以及一个缺少了C端的NTR结构域的NET1(NET1NTR)组成,这也与之前的研究结果一致。
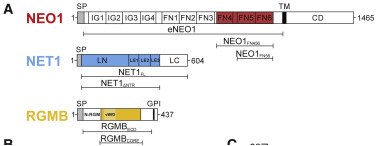
图2 NEO1、NET1、RGMB的示意图
由于细胞可以在体内以依赖NEO1 的方式同时遇到 RGM 和 NET1,作者探究细胞表面是否存在稳定的三元NEO1-NET1-RGM复合物,或者NET1和RGM是否会竞争结合NEO1。为了探究这两种区别,作者采用Proximity Ligation Assay(PLA)实验,将经过细胞表达并纯化的全长的NEO1与NETNTR以及全长的胞外RGMB进行相互培养,观察到遇到PLA现象,并且只有当NET1与RGMB非常接近且距离<40nm时才会产生。当RGMB突变为不可链接NET1时,PLA现象明显减少。结果表明,NEO1是连接NET1和RGMB所必需的,并且会在细胞表面形成三元复合物。
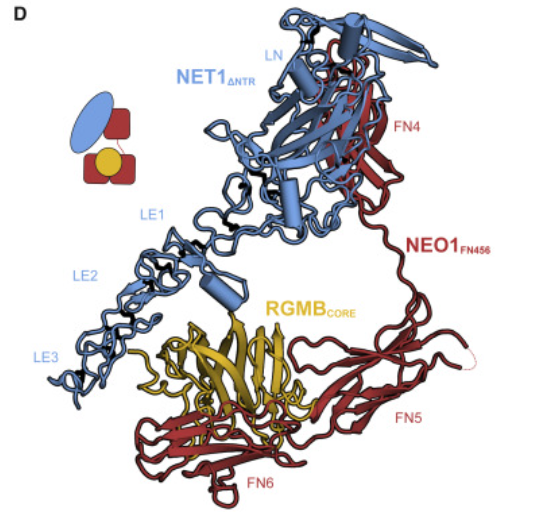
图3. NEO1-NET1-RGMB三聚体
为了揭示NEO1、NET1以及RGMB如何组装成三元复合物,作者收集到复合物分辨率为3.25A晶体结构,并通过超速离心分析(AUC)和小角度X射线散射(SAXS)分析了“3-3”三聚体的溶液稳定性,最终确定了超级复合体3:3:3NEO1-NET1-RGMB的基本组成。
“3-3”超级复合体的主体本质上是由NEO1和NET1之间的相互作用形成的。NET1是细长的且刚性的分子,使得与两个相邻NEO1分子接触,以弥合超复合物。冷冻电镜结果显示,有四个N连接上蔗糖,另外有四个位置通过非共价连接了八硫酸酯盐(SOS)分子,蔗糖八硫酸酯协助确认三元聚合物超级复合体比例。NET1和RGMB分子形成非常小的相互作用,同时也未观察到NET1与溶液中RGMA以及RGMB的相互作用。这也表明了NET1-NEO1相互作用是形成“3-3“超级复合体的驱动力。
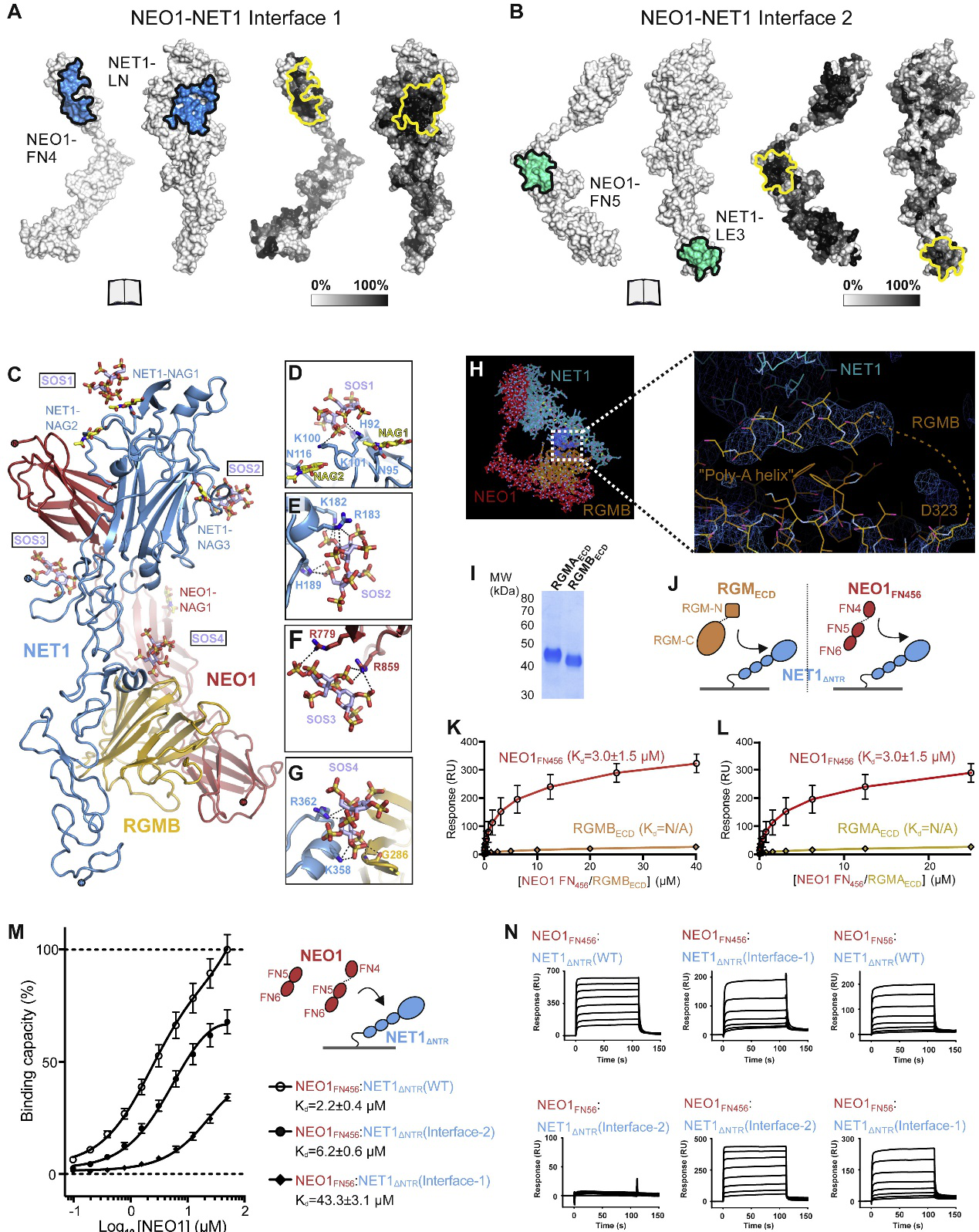
图4. 三元NEO1-NET1-RGM复杂聚合物的功能性分析
(C、D、E、F、G详细标明蔗糖八硫酸酯盐在复杂三聚体表面的结合位置)
之前的研究结果表明,RGMB对DCC的结合亲和力比NEO1低约1000倍。在该研究中该研究团队显示在CNs中敲除DCC对RGMA诱导的生长锥塌陷没有影响,也没有影响NET1调节这种效应的能力。DCC缺失不影响NET1介导的神经细胞迁移,也不影响RGMA或RGMB抑制这种作用的能力。这支持RGM抑制可能归因于三元NEO1-NET1-RGM复合物的观点。NEO1与DCC一起的不同进化可以通过信号转导中对三元NEO1-NET1-RGM复合物的需求来解释。
该研究团队的研究表明,NET1可以沉默RGMA介导的中枢神经系统生长锥塌陷,需要NEO1,RGMA和RGMB抑制NET1对神经细胞迁移的积极作用。NET1介导的神经细胞迁移在体外以剂量依赖性方式被RGMA抑制。这些数据表明NET1和RGMA和RGMB在功能上相互作用,并且它们的同时呈现导致其下游效应的相互沉默,这与三元复合物起到沉默受体信号传导的作用一致。
该实验也拓宽了蔗糖八硫酸酯盐的应用范围,在制备冷冻电镜样品或蛋白质修饰中均存在一定的应用价值。由于其独特的负电性,可以在蛋白表面寻找可能的结合位点,并且通过分子量变化,进而确定多聚体蛋白质的组成,确定蛋白质复合物的各组分比例,为探索蛋白间的相互作用提供可能。
[1] Robinson RA, Griffiths SC, van de Haar LL, et al. Simultaneous binding of Guidance Cues NET1 and RGM blocks extracellular NEO1 signaling. Cell. 2021;184(8):2103-2120.e31. doi:10.1016/j.cell.2021.02.045


