《mRNA-LNP疫苗的结构与稳定性》文献解读系列四
文章来源:AVT发布时间:2021-09-02浏览次数:
mRNA疫苗的体外稳定性
正如之前在背景介绍中提到的,目前已批准的 mRNA疫苗流通的主要障碍之一是它们必须以冷冻形式储存。在 2–8 °C 的温度下,辉瑞/BioNTech 和 Moderna 疫苗分别可稳定保存 5 天和 30 天,两家公司都为终端使用提供了详细的处理说明。有趣的是,据报道 CureVac 的候选疫苗在冰箱温度和 -60 °C 下可稳定 3 个月。这些是目前发布了mRNA-LNP长期储存条件的制造商,这种苛刻的温度要求严重影响了这些疫苗的储存、运输和流通。然而,迄今为止,在公开资料中几乎没有关于优化mRNA 疫苗稳定性的信息。本节旨在概述影响 mRNA-LNP 疫苗成分稳定性的因素,并讨论分析评价这种稳定性的方法。
mRNA稳定性
强烈影响所需储存条件的主要因素是 mRNA 的稳定性。如上文2.1 节所述,mRNA 分子的结构经过专门设计可以用于增加体内靶抗原的翻译。mRNA 的特殊性在于,即使是长 mRNA 链(通常长度在 1000 到 5000 个核苷酸之间)中的一个核苷酸发生变化(链断裂或碱基氧化)便会导致翻译终止。这使得 mRNA 疫苗与其他疫苗完全不同,在其他疫苗中,抗原的微小变化不一定对其功效产生显影响。因此,对于 mRNA 疫苗,监测整个分子的完整性是至关重要的。
mRNA 降解的方式有多种,可以分为化学和物理降解。化学降解包括 mRNA 分子中化学键的改变。物理不稳定性包括变性(二级和三级结构的丧失),与变性对蛋白质生物制剂活性的影响不同,物理不稳定性对mRNA的影响可能不太明显。然而,变性还包括聚集和沉淀等变化,这些变化会影响mRNA的翻译表达。在一篇关于核酸稳定性的综述中,Pogocki 和 Schöneich 指出化学降解在siRNA降解中的影响比物理不稳定性更大,对于链长更长的 mRNA来说可能更是如此。
mRNA在体外的化学降解主要包括水解和氧化,水解主要是发生在mRNA 分子骨架的磷酸二酯键(图5 )。核糖上的2' OH 基团起着至关重要的作用,因为导致 mRNA 链断裂的酯交换反应起始于磷酸酯键上的 2'OH 基团的亲核进攻导致 P-O5' 酯键断裂(图5)。这个过程需要水,可以被核酸酶催化,也可以被 mRNA 分子本身和其他外源因素如酸和碱催化。在有关 mRNA 水解的两篇文献中,作者指出 mRNA 的碱基序列和二级结构会影响水解速率。具体而言,碱基堆积可能会降低磷酸二酯键的裂解速率,可以小化 mRNA 分子的“平均未配对概率”。可以使用专门设计的算法来选择可以形成大双链区域的单链 mRNA 的核苷酸序列。据称,采用这种方法优化后,体外稳定性得到了改善。
CureVac、辉瑞/BioNTech 和 Moderna 疫苗之间的区别在于后两者具有 1-甲基-假尿苷的单核苷掺入。之前的一项研究表明,这种修饰提高了 RNA 二级结构的稳定性。CureVac 采用提高GC比例策略,具有类似的效果。
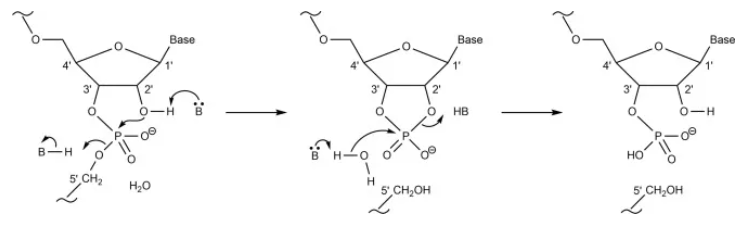
图5 通过 2',3'-环状磷酸酯,碱基催化RNA分子内的磷酸二酯键水解、B表示Brønsted碱。
相反,氧化会影响碱基,并在较小程度上影响mRNA 核糖单位的糖基团。氧化可导致碱基裂解、链断裂和 mRNA 二级结构的改变。然而,如前所述,水解似乎被认为是驱动 mRNA 降解的关键因素。
原文文献:
Linde,S;Dominik ,W;Jayesh A. K;Rein ,V;Gideon ,K;Wim ,J;Daan J.A. C.mRNA-lipid nanoparticle COVID-19 vaccines: Structure and stability.International Journal of Pharmaceutics.2021,601,120586
参考文献来源:
1. Abdelwahed, W., Degobert, G., Stainmesse, S., Fessi, H., 2006. Freeze-drying ofnanoparticles: Formulation, process and storage considerations. Adv. Drug Deliv.Rev. 58 (15), 1688–1713. https://doi.org/10.1016/j.addr.2006.09.017.
2. Yanez Arteta, M., Kjellman, T., Bartesaghi, S., Wallin, S., Wu, X., Kvist, A.J.,Dabkowska, A., Sz´ekely, N., Radulescu, A., Bergenholtz, J., Lindfors, L., 2018. Successful reprogramming of cellular protein production through mRNA delivered
by functionalized lipid nanoparticles. Proc. Natl. Acad. Sci. U. S. A. 115 (15),E3351–E3360. https://doi.org/10.1073/pnas.1720542115.
3. Ayat, N.R., Sun, Z., Sun, D.a., Yin, M., Hall, R.C., Vaidya, A.M., Liu, X., Schilb, A.L.,Scheidt, J.H., Lu, Z.-R., 2019. Formulation of biocompatible targeted ECO/siRNAnanoparticles with long-term stability for clinical translation of RNAi. Nucleic AcidTher. 29 (4), 195–207. https://doi.org/10.1089/nat.2019.0784.
4. Baden, L.R., El Sahly, H.M., Essink, B., Kotloff, K., Frey, S., Novak, R., Diemert, D.,Spector, S.A., Rouphael, N., Creech, C.B., McGettigan, J., Khetan, S., Segall, N.,Solis, J., Brosz, A., Fierro, C., Schwartz, H., Neuzil, K., Corey, L., Gilbert, P.,Janes, H., Follmann, D., Marovich, M., Mascola, J., Polakowski, L., Ledgerwood, J.,Graham, B.S., Bennett, H., Pajon, R., Knightly, C., Leav, B., Deng, W., Zhou, H.,Han, S., Ivarsson, M., Miller, J., Zaks, T., 2021. Efficacy and safety of the mRNA-1273 SARS-CoV-2 vaccine. N. Engl. J. Med. 384 (5), 403–416. https://doi.org/10.1056/NEJMoa2035389.
5. Ball, R.L., Bajaj, P., Whitehead, K.A., 2016. Achieving long-term stability of lipidnanoparticles: examining the effect of pH, temperature, and lyophilization. Int. J.Nanomed. 12, 305–315. https://doi.org/10.2147/IJN.S123062.
6. Bloom, K., van den Berg, F., Arbuthnot, P., 2020. Self-amplifying RNA vaccines forinfectious diseases. Gene Ther. 1–13 https://doi.org/10.1038/s41434-020-00204-y.Brader, M.L., Williams, S.J., Banks, J.M., Hui, W.H., Zhou, Z.H., Jin, L., 2021.
7. Encapsulation state of messenger RNA inside lipid nanoparticles. Biophys. J. https://doi.org/10.1016/j.bpj.2021.03.012.
8. Brisco, M.J., Morley, A.A., 2012. Quantification of RNA integrity and its use formeasurement of transcript number. e144–e144 Nucleic Acids Res. 40. https://doi.
org/10.1093/nar/gks588.
9.Burke, P.A., Gindy, M.E., Mathre, D.J., Kumar, V., Prud’homme, R.K., 2013. Preparationof Lipid Nanoparticles. US 2013/0037977.
10. Buschmann, M.D., Carrasco, M.J., Alishetty, S., Paige, M., Alameh, M.G., Weissman, D.,2021. Nanomaterial delivery systems for mRNA vaccines. Vaccines 9 (1), 65. https://doi.org/10.3390/vaccines9010065.


