mRNA-LNP制剂中缓冲体系的筛选与评估
文章来源:发布时间:2023-12-18浏览次数:
上周,艾伟拓产品团队分享了非脂质药用辅料对mRNA-LNP制剂稳定性的影响。(参考阅读:《非脂质药用辅料对mRNA-LNP稳定性的影响及筛选考量》
本周,我们接着这个话题,通过一篇美国俄勒冈州立大学药学院的研究论文,进一步讨论缓冲体系对mRNA-LNP的影响,供大家参考

摘 要
该研究测试了三种常见生物缓冲液——HEPES、Tris和PBS——在单次冻融前后与DLin-MC3-DMA mRNA-LNP制剂的相容性。通过电子显微镜、差示扫描量热法和膜流动性分析发现,不同缓冲液使LNP形态发生了不同的结构变化。采用体外和体内模型测量mRNA转染效率,发现Tris或HEPES缓冲液中的LNPs具有更好的冷冻保护效果以及与PBS相比更高的转染效率
1.缓冲体系可能对LNP的性质与稳定性有较大影响
近年来,脂质纳米颗粒(LNPs)作为treat多种遗传疾病、疫苗和蛋白质替代疗法的非病毒核酸递送平台受到了wide—range关注。COVID-19mRNA-LNP疫苗的全球成功凸显了基于LNP的核酸递送潜力。
LNP配方的优化取决于混合方法,速率,使用的溶剂,pH值中和和纯化过程。
虽然LNPs通常被认为是凝聚态疏水材料,但它们可以捕获大量的水,这取决于LNP的组分和其包载的mRNA分子。mRNA-LNPs水分含量可以高达30%,这表明LNP制剂中缓冲体系的选择可能会对LNP的形成、性质和稳定性产生巨大影响,尤其是考虑到mRNA-LNPs溶液需要在零度以下的温度下长期储存的情况。
缓冲液在冷冻时的结晶会严重影响生物制剂的性质,并会导致LNP破裂和聚集,这在most近的报道中得到了证实。此外,缓冲液在冻结时的一个特殊性质是诱导产生pH梯度。例如,常用的磷酸缓冲盐溶液(PBS)在冷冻时可以经历多达4个单位的pH变化。常见的糖类冷冻保护剂如海藻糖、蔗糖等可以一定程度上抑制这些影响,但无法完全消除。
据报道,磷脂头部基团也会与缓冲体系相互作用,导致脂质膜软化。
因此,LNPs可能高度敏感于pH和膜弹性的动态变化,如缓冲体系类别、离子强度或温度变化。
2该研究中LNP配方及表征方法
将萤火虫荧光素酶(FLuc) mRNA用50 mM柠檬酸钠缓冲液(pH 4)和分子级水稀释,达到所需体积。将DLin-MC3-DMA、DSPC、胆固醇和DMG-PEG-2000溶解在总脂质浓度为5.5 mM的纯乙醇(摩尔比为50:10:38:1.5)中,以3:1的体积比(水/乙醇)和9 mL/min的总流速通过标准微流控混合制备LNPs。
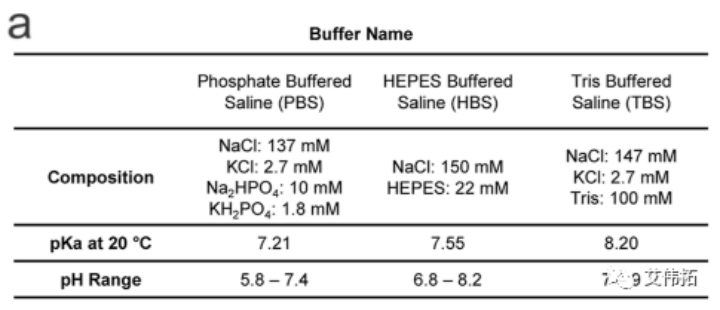
制备用于透析的HEPES、Tris和PBS(详见下图a,Tris即为Tris Buffer,HBS即为HEPES Buffer),其盐度为150 mM, pH为7.4。配制后,立即将LNPs转移到10个kDa MWCO盒中,并在各自的缓冲液中以1000倍的体积透析4小时和过夜。透析后,LNPs在Amicon Ultra离心过滤装置中以3000g离心浓缩,分子量截止为100 kDa(Millipore Sigma, Burlington, MA)。
使用Zetasizer Nano ZSP对LNPs进行了水动力尺寸、多分散性指数和表面zeta电位的表征。对于Zetasizer分析,LNPs在各自的缓冲液中稀释,得到三次测量结果。为了量化mRNA的包封效率和浓度,采用了改进的Quanti-iT RiboGreen RNA(Invitrogen)方案。
3研究成果
3.1 缓冲液对LNP的形成和短期稳定性的影响可以忽略不计
通过标准的微流体混合程序制备含有FLuc mRNA的LNP。DLin-MC3-DMA、DSPC、胆固醇和DMG-PEG-2000脂质按50:10:38.5:1.5摩尔比混合,pH 4柠檬酸缓冲液中的mRNA溶液与乙醇脂质混合物的体积比为3:1,总流速为9 mL/min。然后将所得的LNP悬浮液分成三等份,分别与PBS、Tris或HEPES进行透析。
透析后,将LNPs浓缩,并通过动态光散射(DLS)和改进的核糖绿测定法进行分析。
DLS分析显示,三种缓冲液中LNPs颗粒大小几乎相同,约为70 nm,PDI约为0.05。
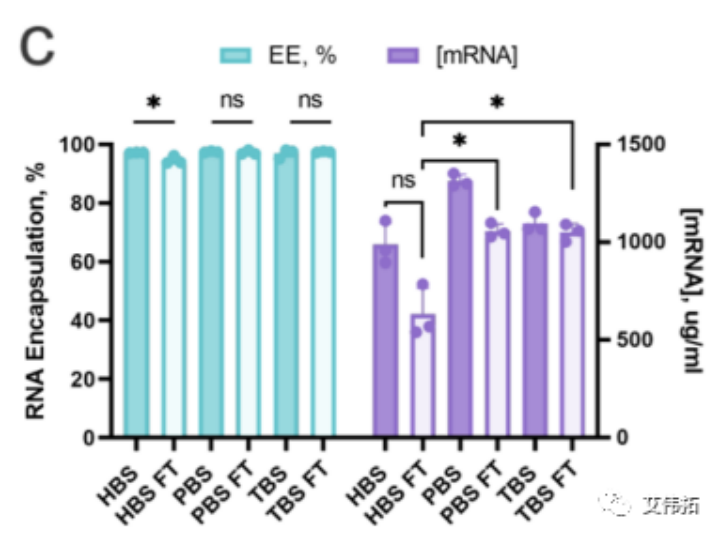
Zeta电位值表明,PBS和Tris配方的表面电荷略为负(约−3mV),HEPES配方的表面电荷为中性,三种缓冲液中包封率均为>92%。
LNP的冷冻透射电镜显微照片也没有显示任何outstanding的形态变化,这表明缓冲液对LNP的形成、形态或短期稳定性的影响可以忽略不计。
3.2 低温冻存复溶后,不同缓冲液中LNP关键表征出现差异
在- 20℃下保存三周后,将不同缓冲溶液中的LNPs在室温下解冻30分钟,立即用于研究。
①粒径
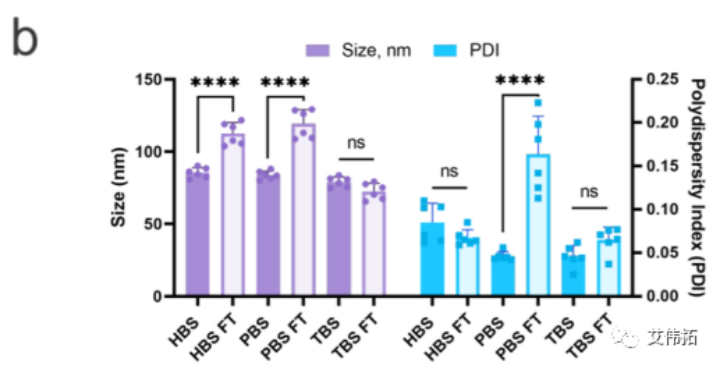
储存在HEPES和PBS中的样品在FT后的平均粒径增大了约50%,而储存在Tris中的LNPs的粒径减小了约10 nm。
②PDI
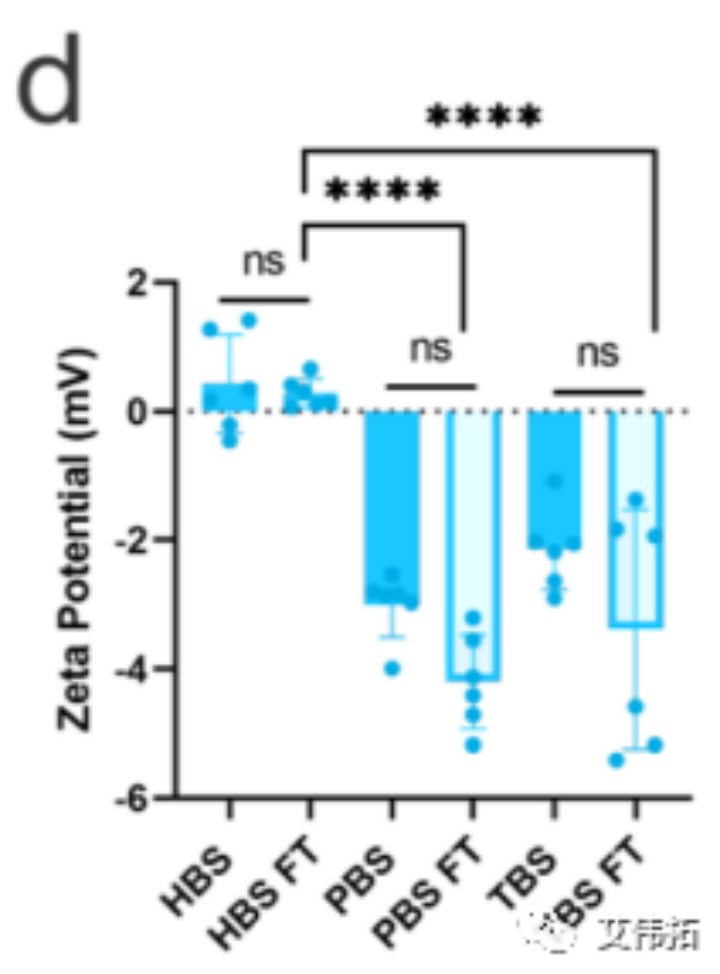
HEPES和Tris中LNPs的PDI在冻融前后基本保持一致,而PBS中LNPs在解冻后PDI增加了3倍(上图b)。FT后Zeta电位也略有下降(上图d)。
③LNP形态
LNP形态受到冻融的严重影响,冷冻透射电镜证实PBS缓冲液中的 LNP在大小上most多样化,并且显示出高度异质性的内部组织,以及颗粒聚集。这可能是脂质相和水相分离所导致。具体而言,PBS中的LNP包含典型的100 nm以下的致密LNPs,100~150nm的空脂质体样结构,以及不同粒径包载水相的LNPs,其中部分水相中含有mRNA。
DLS分析显示,Tris中的LNPs尽管观察到形态变化,但尺寸和PDI没有明显变化,这表明相比于PBS,Tris可能可以更大程度地抑制LNPs颗粒的聚集。
与新鲜LNPs相比,HEPES中的LNPs在冻融后出现独特的沙漏状结构,尺寸略大(见下图e)。在LNPs周围形成的水泡似乎缺乏mRNA,这可能表明HEPES可以影响mRNA周围脂质的堆积,例如,HEPES可以促进脂质与mRNA之间更强的静电相互作用——HEPES LNPs的zeta电位是真正的中性的,而PBS和Tris LNPs具有−2至−5 mV的轻微负电荷,这可能表明当HEPES存在时,mRNA电荷的中和作用更有效。

此外,基于冷冻显微图像研究了脂质膜厚度的变化。
平均而言,脂膜厚度在FT后增加了15%,表明膜水合作用增加。
更具体地说,冷冻后,Tris LNPs的脂膜厚度增加了约0.8 nm, PBS增加了约0.6 nm, HEPES LNPs增加了约0.2 nm。尚不完全清楚这些改变是否表明脂质膜成分发生变化或onlyonly是水掺入的结果,但这些结果突出了解冻后LNPs的脂质膜发生了outstanding变化,且不同缓冲体系中变化程度不同。
以上实验结果表明,不同缓冲液对mRNA-LNPs的关键表征(形态、粒径、PDI,脂质膜厚度等)可以产生较大影响。
3.3 转染能力与内涵体逃逸的体外评估
①缓冲液影响LNP转染能力
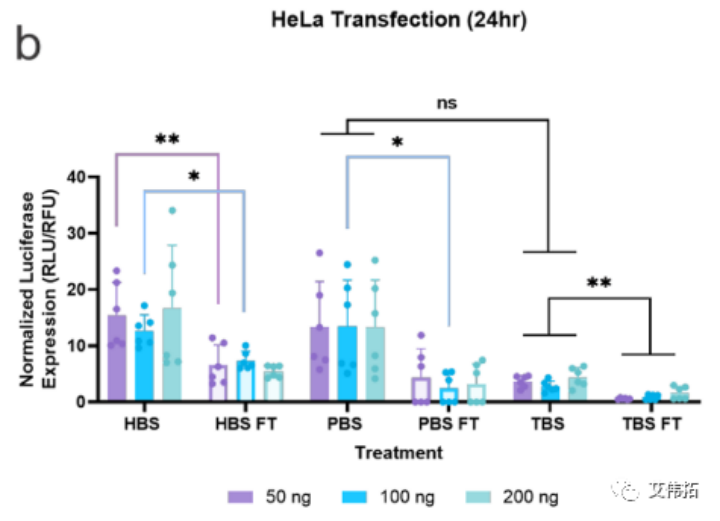
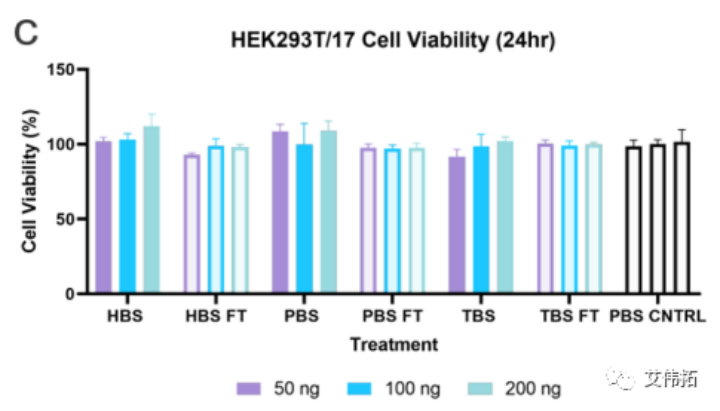
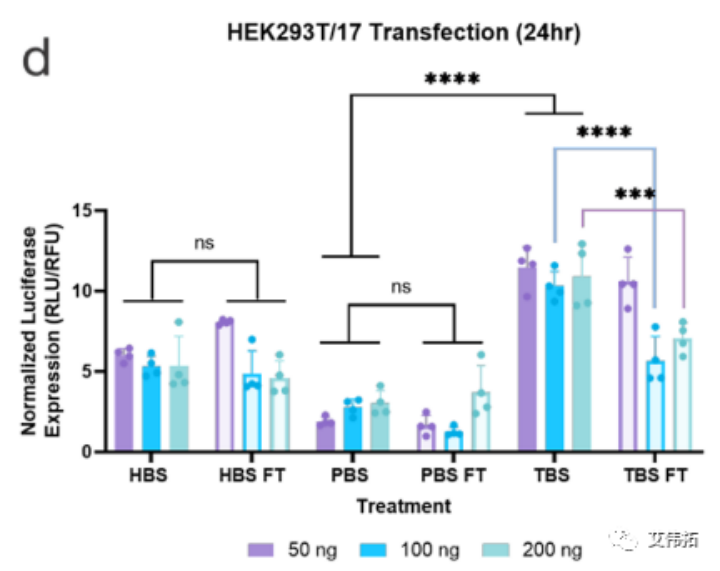
该研究评估了不同缓冲液中的LNPs的转染能力和内涵体逃逸的程度。分别用包封FLuc mRNA的LNPs处理hela和HEK293T/17(后者用Gal9-GFP报告系统修饰)两个细胞系,并在24小时后检测。无论使用何种缓冲液,细胞存活率均保持在80%(下图a,c)。转染评价表明,缓冲液的转染效率随细胞系的不同而变化。在HeLa细胞中,LNPs转染趋势为HEPES>PBS>Tris(下图b),而HEK293T/17细胞表现出Tris>HEPES>PBS的偏好(下图d)。
一般来说,所有的mRNA-LNP制剂在解冻后转染效果都有所下降。在HeLa细胞中,PBS LNPs的转染效率下降most为严重,在所有处理中平均下降4倍,而HEPES在所有处理中平均下降2倍(下图b)。对于HEK293T/17细胞系, HEPES和PBS LNPs均无统计学意义的下降,而Tris在100和200 ng时的LNPs分别下降了2 ~ 2.5倍(下图d)。

②缓冲液影响内涵体逃逸效率
凝集素是一个与病原体入侵和免疫感知相关的糖结合凝集素家族。半乳糖凝集素如gal3、gal8和gal9从弥漫的细胞质表达重新分布到暴露的糖苷位点,这是由于内体内小叶暴露事件造成的,表明内涵体破坏。Gal9已被证明在报告细胞内涵体逃逸的检测中具有most高的信噪比。因此,可利用Galectin 9 (Gal9)- gfp 修饰的HEK293T/17细胞系,评估FLuc mRNA LNPs的内涵体逃逸情况。
低剂量处理(50 ng)在所有新鲜LNPs中几乎没有变化,HEPES LNPs在FT后表现出most高的Gal9募集和mostoutstanding的变化(2.6倍)。
高剂量(200ng)处理组中,冷冻前Tris LNPs诱导了most高的Gal9募集。不同缓冲体系中的LNP对FT的反应完全不同。PBS LNP减少了Gal9的招募,Tris LNPs几乎没有变化,HEPES LNPs增加了Gal9的招募。解冻后的HEPES LNPs内涵体逃逸的增加可能是低温透射电镜观察到的形态学变化的结果。LNP形态的变化导致体外转染的增加,因此HEPES可能促进了解冻后LNP形态的有利变化。
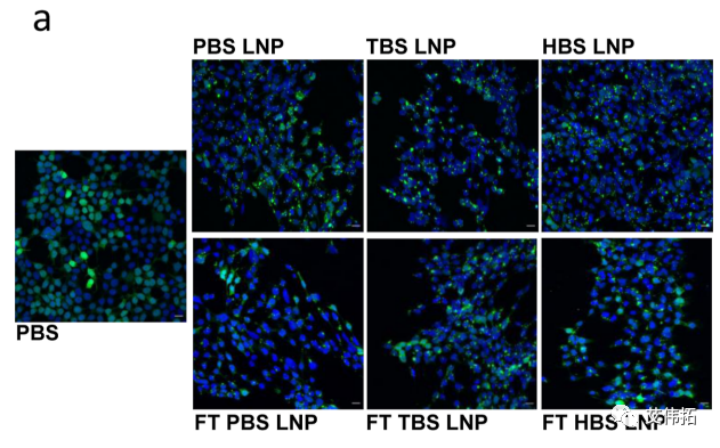
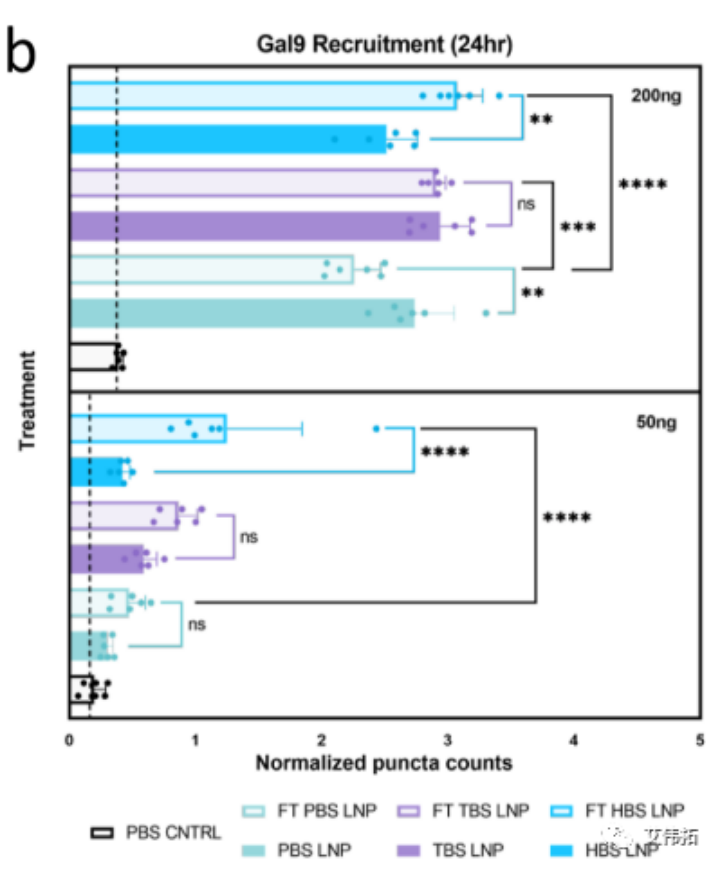
这些体外实验数据进一步支持了LNP缓冲液组成对冻融后转染效率的重要性,并揭示了细胞摄取的差异受到这些变化的影响。
3.4 体内成像评估mRNA表达情况
通过living body成像,探索了不同缓冲体系mRNA-LNP在体内的表达情况。将HEPES、Tris和PBS LNPs静脉注射到年龄匹配的雌性BALB/c小鼠中,比较荧光素酶的表达水平和apparatus特异性。在注射后4和24 h时间点测量新鲜和解冻的LNPs的生物发光信号。
在所有案例中,生物发光图像显示强烈的肝脏转染模式,与通常的LNP静脉注射制剂一致。

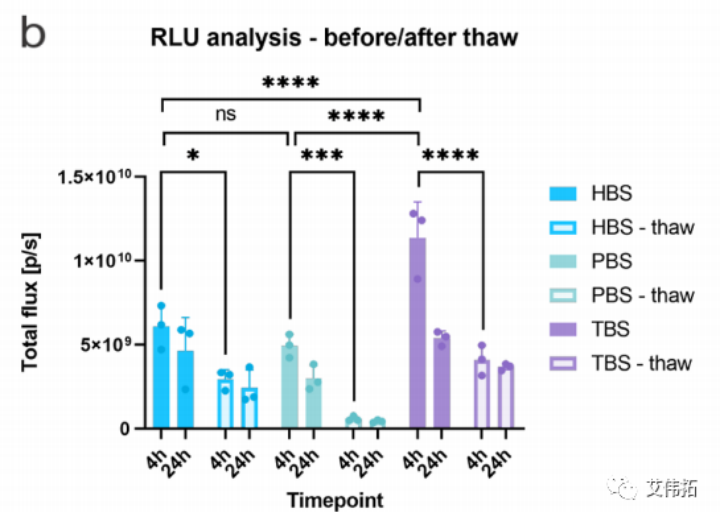
总体而言,HEK293T/17细胞系的体内转染趋势与体外观察到的相似(Tris > HEPES > PBS)。新鲜LNPs之间的交叉比较得出结论,与其他缓冲液相比,Tris组在给药后4小时增加了2倍。这种功效的增强可能是由于脂质膜上的水置换改善了apoe介导的摄取,正如脂质膜厚度减少所表明的那样。
然而,缓冲液导致了不同程度的转染损失。对于给药后4小时的FT组,HEPES显示总通量减少约2倍,Tris显示减少约3倍,PBS (LNP配方中most常见的缓冲液)导致总通量减少近9倍。
有趣的是,在24小时时间点,不同缓冲液样品之间mRNA表达水平没有统计学上的outstanding差异。这可能是LNPs在血液中不断循环,缓冲液作用减弱的结果。
总的来说,与先前的观察结果一致,mRNA的传递受到冻融过程的影响。缓冲液对体内给药效果的巨大影响表明,在LNP制备中选择适宜的生物缓冲液,或可为保持mRNA-LNP的理化性质及生物学活性提供outstanding优势。
4
结论
脂质纳米颗粒(LNP)通常通过透析或与生理缓冲液(如PBS)交换缓冲液来中和,纯化后可直接注射入生物体。此外,缓冲体系可以作为冷冻保护剂,减轻LNP制剂在低温储存时的稳定性问题。
值得注意的是,FDA批准的COVID-19疫苗Spikevax和Comirnaty使用不同的缓冲液,这表明不同的mRNA-LNP制剂可能对缓冲体系有不同的要求。(笔者注:Comirnaty上市后制剂prescription中缓冲体系由PBS变更为了Tris,详细信息请参考:《Moderna:使用TRIS缓冲体系可提高mRNA稳定性》)
因此,为LNP制剂筛选适宜的缓冲体系是一个极具价值的研究课题。然而,缓冲体系对LNP的结构形态、包封率和转染效率方面的作用迄今尚未得到充分研究。
本文分享的研究中,使用常用阳离子脂质DLin-MC3-DMA制备mRNA-LNP,在-20℃低温冷冻3周,比较了LNP冻存前后的理化性质和生物学活性(体外+体内)。
结果表明,通过体外和体内转染衡量,在HEPES和Tris体系中的LNPs总体上优于PBS。与PBS相比,HEPES和Tris作为冷冻保护剂,可以在更大程度上保存LNPs的结构和mRNA的递送效率。
此外,储存在HEPES中的LNPs在FT循环后形成了独特的沙漏状结构,而Tris和PBS在冻融后都产生了高度聚集的结构。因此,HEPES可以为LNPs提供更好的保护,防止pH梯度急剧下降,防止LNP聚集,most终控制相分离过程。另一方面,使用Tris对转染特别有益,这表明缓冲盐等辅料在LNP制剂中的作用可能被much低估了。
通过分享该研究,艾伟拓产品团队希望揭示LNP制剂prescription研发过程中,缓冲体系选择的重要性,希望能够为广大核酸递送企业及相关从业者带来一定的参考。
未来,艾伟拓产品团队也会持续关注核酸递送制剂prescription相关研究进展,包括不同剂型(如冻干剂型)、不同存储条件(如2~8℃冷藏存储)、不同LNP脂质组分及不同载荷等因素对LNP制剂辅料选择的影响。
下一期,艾伟拓产品团队将为您带来《冷冻或冻干导致pH值变化及对应缓冲体系筛选考量》,敬请期待!
如需了解更多相关信息,您也可以与所在区域艾伟拓销售人员联系,或扫描下图中的二维码联系我们,预约艾伟拓产品团队的专场报告!

艾伟拓近20年来始终专注于high-end注射级辅料,长期稳定供应注射级TRIS/TRIS-HCl、HEPES等生物缓冲体系,具有GMP条件生产,中美双报,供注射用,ultralow内TOXIN,DNase& RNase free,符合国际主流药典标准,现货快速供应等优势,助力mRNA疫苗等核酸制剂的研发生产与中外申报!


